治験とは?近年注目されているバーチャル治験についても解説 #026

2022.12.23
2025.03.27
治験の流れや非臨床試験・臨床試験、新薬ができるまでについて、わかりやすく解説します。また、「バーチャル治験」という言葉を耳にしたことはあっても、詳細を知らないという方もいるでしょう。
この記事では、「バーチャル治験」の概要やメリットも詳しくまとめているので、ぜひご一読ください。
目次
治験とは

治験とは、新しい薬として国から承認を得るために主に病院で実施する臨床試験のことです。実際に患者や健康な成人に薬を使用して、効果や安全性を確認します。
製薬会社は治験の結果を厚生労働省に提出します。その後、国の審査・承認を経てから新しい薬が誕生し、多くの人に使われるようになるのです。
なお、治験を実施するのは、「医薬品の臨床試験の実施の基準に関する省令」の第三十五条で定められた要件を満たした医療機関のみです。また、治験の責任者も第四十二条で定められた要件を満たした医師と決められています。
臨床試験とは
臨床試験とは、新しい薬や医療機器、治療法などの効果・安全性を確認するために実施される試験のことです。臨床試験のなかでも、新しい薬として国から承認を得るために、「ヒト」を対象として医療機関で実施する試験のことを治験といいます。
新しい薬の研究・開発をして市場に出すには、「医薬品の臨床試験の実施の基準に関する省令」に基づいて、非臨床試験と臨床試験を実施する必要があります。
非臨床試験
「動物」を対象として実施する試験のことを、非臨床試験といいます。
治療で使用される医薬品は、植物由来成分や土壌中の菌、微生物から発見された成分のほか、化学合成で生成された化学物質、バイオテクノロジーによって精製された物質からつくられています。これらの成分・物質を人に対して有益と仮定した場合、どのような効能や安全性、有毒性があって、なおかつ実現可能かを調べるために「動物」を対象として試験を実施します。
試験の対象となる動物は、マウス・ラット・モルモット・ウサギ・イヌ・ブタなどです。
臨床試験
「動物」を対象とする非臨床試験を経て実施される、「ヒト」を対象とした試験のことを臨床試験といいます。
臨床試験では非臨床試験で得られた薬理作用や薬物動態、有害事象などに関するデータに基づき、「ヒト」を対象とした場合に効能や効果が期待できる薬の候補を選びます。そして、その薬の候補を実際に「ヒト」に使用して、有効性や安全性、用法、容量を確認します。
臨床試験は、第I相試験・第II相試験・第III相試験の3段階を踏んで進められます。
新薬ができるまで
新薬は、以下5つのステップを踏んで完成します。
- 基礎研究
- 非臨床試験
- 臨床試験
- 審査・承認
- 製造販売後調査
以下で詳しく解説します。
1. 基礎研究
新薬を作る最初のステップである基礎研究では、植物由来成分や土壌中の菌、微生物、海の生物などから薬の候補となる成分を探し、構造や性質、状態について調べます。
基礎研究に要する期間は、2~3年ほどです。
2. 非臨床試験
成分や物質の研究が終わったら、「動物」を対象とした非臨床試験を実施します。非臨床試験では、以下のような研究を実施します。
- 薬効薬理研究
どれくらいの量でどの程度の効果があるのか、どのような方法で使用するのかを調べる - 薬物動態研究
薬が体内にどのように吸収されるのか、血液を通してどのように組織全体にまわるのか、肝臓で代謝されて排出されるかを調べる。また、薬物相互作用(飲み合わせ)も調べる - 一般薬理研究
体内のどのような部位にどういった作用を及ぼすか調べる。また、薬効薬理作用以外の安全性についても調べる - 一般毒性・特殊毒性研究
投与期間を短期間・中期間・長期間に分けて、安全性・毒性を調べる。また、発がん性や胎児への影響がないかも調べる
非臨床試験では3~5年ほどかけて、効能や安全性、有毒性を確認します。
3. 臨床試験
「動物」を対象とする非臨床試験で実現可能か確認できたら、「ヒト」を対象とした臨床試験を実施します。臨床試験は、以下の3段階を踏んで進められます。
- 臨床第I相試験(臨床薬理試験)
少数の健康な成人に薬を使用して、安全性や薬物動態を調べる - 臨床第II相試験(探索的試験)
少数の患者に薬を使用して、有効性や安全性などを調べる - 臨床第III相試験(検証的試験)
多数の患者に薬を使用して、有効性や安全性などを調べる
臨床試験では健康な成人や患者を対象に、3~7年ほどかけて薬の効能や安全性、用法、容量を確認します。
4. 審査・承認
臨床試験を終えて効果や安全性が確認できたら、厚生労働省に承認申請をします。厚生労働相の諮問機関である「薬事・食品衛生審議会」で審議され、承認までに1〜2年ほど要します。
医薬品製造販売の承認が下りてはじめて、医薬品として扱われます。
5. 製造販売後調査
医薬品として販売され、広く使われるようになった後も、引き続き薬の効果や安全性などを調べます。販売後は、臨床試験よりもさらに多くの患者に薬を使用できます。多くの患者に使用して得られた有効性や安全性などのデータを製薬会社にフィードバックし、薬の改良や開発に活かします。
治験の流れ
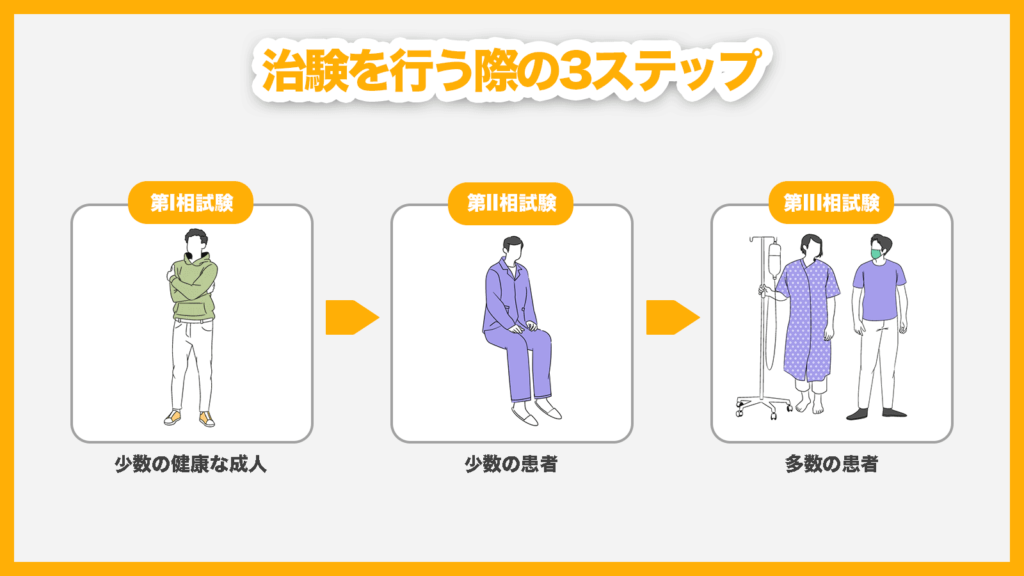
治験は「第I相試験」「第II相試験」「第III相試験」の3つのステップを踏んで進められ、完了するまでに3~7年ほどの期間を要します。
以下では、それぞれの試験の対象者および試験内容を解説します。
1. 第I相試験
第I相試験では、少数の健康な成人に治験薬を使用して安全性や薬物動態を調べます。薬の投与・服薬は実際に想定される使用量よりもごく少量からはじめ、少しずつ量を増やしていきます。
健康な成人を対象とするのは、副作用が起こった場合に治験薬によるものなのか、それとも対象者が元々飲んでいた薬との飲み合わせによるものなのか判断できないためです。できる限り同じ条件下で治験薬の安全性や薬物動態を調べるために、まずは健康な成人でチェックします。
2. 第II相試験
第II相試験では少数の患者に治験薬を使用して、どれだけ効果が優れているかを調べます。どの程度の量をどのタイミングで投与・服用すると、最も効果的で副作用が少ないのかを調べます。
有効性や投与方法などを調べる際には、投与量を変えて比較検討します。第II相試験は、「探索的臨床試験」とも呼ばれています。
3. 第III相試験
第III相試験では、第I相試験と第II相試験のデータをもとに多数の患者に治験薬を使用して、どれだけ効果が優れているかを調べます。治験薬と対照薬(現在治療で使われている標準的な薬)を比較するほか、先入観や思い込みで結果が変わることのないよう、有効成分を含んでいないプラセボ(偽薬)を用いて効果を調べるのです。
なお、より多数の患者に使用することで、最終的な安全性も確認します。
いま注目されるバーチャル治験
近年は、バーチャル治験が注目されています。
新型コロナウイルス感染症が流行したことにより、医療現場ではオンラインで診療や薬の処方をするようになりました。デジタル化の波は医療現場だけでなく、医薬品の開発現場でも進んでいます。
治験は基本的に医療機関で実施されるため、被験者は医療機関に行かなくてはならず、入院が必要な場合もあります。通院や入院は被験者にとって負担が大きいため、なかなか被験者が見つからず、治験が進まないことがありました。
厚労省では「被験者が集まらず治験が進まない」という問題を解決すべく、被験者の来院に依存しない治験(分散型臨床試験:DCT)を国内で実施できるよう、規制の整備を進めています。
バーチャル治験とは
バーチャル治験とは、被験者が来院せずとも自宅で受けられる治験のことです。バーチャル治験は、以下のシステムやツールなどを活用して実施されます。
- eConsent
治験への同意を得るために、説明や同意を電子的に取得するシステムのこと - オンライン診療
パソコンやスマートフォンといった電子機器のカメラ通話機能を使用して、オンラインで医師の診察や薬剤処方などを受けられる診療のこと - ウェアラブルデバイス
生体情報や運動情報を取得するために腕や脚、頭などに装着するコンピューターデバイスのこと - ePRO(電子患者報告アウトカム)
患者がスマートフォンやタブレット端末などを通じて記録した健康状態を、医療者がリアルタイムに評価できるシステムのこと
バーチャル治験のメリット
バーチャル治験は通院必須ではないため、一般的な治験よりも被験者が集まりやすく、治験を実施しやすいのがメリットです。また、被験者に通院や入院の負担がないため離脱率も下がるでしょう。
結果的に、新薬の誕生までの期間が短くなることが予想されます。
なお、被験者は治験中もいつもと同じ生活を送るため、医療機関という非日常空間におけるデータではなく、日常生活に沿ったリアルなデータを収集できます。ウェアラブルデバイスやePROを活用することで、被験者の日常生活における健康状態や運動量といったデータも収集可能です。
バーチャル治験を実施することで、今後は患者の日常を反映した医薬品の開発も期待できるでしょう。
まとめ
新薬は開発から承認までに9~17年ほどかかり、治験だけでも3~7年ほどを要します。治験は基本的に医療機関で実施されるため、被験者は通院や入院が必要で治験を実施するハードルが高いのが現状です。
しかし、近年は被験者が来院せずとも自宅で治験を受けられるバーチャル治験に注目が集まっています。バーチャル治験は被験者を集めやすく開発期間を短縮できるのがメリットです。
厚労省では、被験者の来院に依存しない治験(分散型臨床試験:DCT)を国内で実施できるよう、規制の整備を進めているため、今後も動向に注視しましょう。
メディカル・データ・ビジョン株式会社では、診療データベースで患者数や処方量などを分析するツールやオンコロジー領域に特化した分析ツールなどのサービスを提供しています。また医療データを用いた治験・臨床研究への活用を行っています。ぜひ一度ご相談ください。





