オーファンドラッグとは?指定基準や手続き、近年承認された事例について解説 #94

2025.04.18
2025.04.21
オーファンドラッグとは希少疾病用医薬品のことで、患者数が 少なく、難病のように治療が難しい疾患に 用いられる医薬品です。どのような病気であっても治療に医薬品は欠かせませんが、治療方法が確立されていない難病などの場合、開発に掛かるコストを回収できないという懸念があり、かつてはなかなか開発が進んでいませんでした。その問題を解決するために導入された制度が、オーファンドラッグ制度です。
本記事ではオーファンドラッグの概要やオーファンドラッグ指定の詳細、指定基準や手続き、近年承認された事例などを解説します。オーファンドラッグ指定の基準を満たせば助成金を受けられるため、開発する製薬会社の負担を軽減しながら、必要な方に薬を届けることが可能です。本記事を参考にしてオーファンドラッグへの理解を深めましょう。
目次
オーファンドラッグとは
オーファンドラッグは日本語で希少疾病用医薬品と呼ばれ、患者数が少なく、治療法の確立に至っていない難病などの治療に用いられる医薬品のことを指します。
医薬品を開発するには膨大な費用と時間を要するため、患者数が少なく、 難病のように治療方法が確立されていない疾患に用いる医薬品の場合、開発コストの回収が見込めず、なかなかスムーズに開発が進まないという問題がありました。
しかし患者数の少ない病気であっても、実際にその病気に罹患している患者にとって医薬品の必要性は高いので、日本は1993年に希少疾病用医薬品・希少疾病用医療機器などの研究開発促進制度を導入し、スムーズな開発が行えるように体制を整えています(※)。
※参考:国立研究開発法人 医薬基盤・健康・栄養研究所.「平成29年度希少疾病用医薬品 希少疾病用医療機器 希少疾病用再生医療等製品の開発振興事業について」.P4(2024-06-14)
オーファンドラッグ指定とは何か
オーファンドラッグ指定とは、患者数が少なく、難病のように 治療の難しい 疾病 に用いる薬として、厚生労働大臣から指定を受けることです。オーファンドラッグ指定を受けると、医薬基盤・健康・栄養研究所を通じて医薬品開発のための助成金が受けられる他、以下のような支援措置が受けられます。
- 厚生労働省、医薬品医療機器総合機構(PMDA)、医薬基盤・健康・栄養研究所からの指導や助言
- 助成金の交付対象期間中に実施する試験研究に係る費用の税制措置
- 医薬品の承認審査の優先
- 希少疾病用医薬品に承認された場合の再審査期間の延長
このように医薬品の開発に対しさまざまな支援が受けられるため、製薬会社は負担を軽減しながら更なる開発を進めることができます。
オーファンドラッグの指定基準
オーファンドラッグ指定は医薬品の開発を後押しする制度ですが、どのような医薬品でもオーファンドラッグ指定を受けられるわけではありません。オーファンドラッグの指定基準は、医薬品医療機器法第77条の2に基づいて以下のように定められています(※)。
- 日本において該当の医薬品を必要とする患者数が5万人未満
※難病指定の治療に用いる場合は、難病の患者に対する医療等に関する法律(難病法)第5条第1項で規定する人数まで - 代替となる医薬品や治療法がない
- 既存の医薬品と比べて高い有効性や安全性が期待できる
- 対象となる疾病に対して、該当の医薬品を使用する理論的根拠があり、開発計画の妥当性が認められる
上記の条件を満たす医薬品の申請を行って承認を受けた場合のみ、オーファンドラッグ指定を受けることができます。
※参考:厚生労働省.「希少疾病用医薬品・希少疾病用医療機器・希少疾病用再生医療等製品の指定制度の概要」(2024-05-31)
オーファンドラッグの指定までの手続き
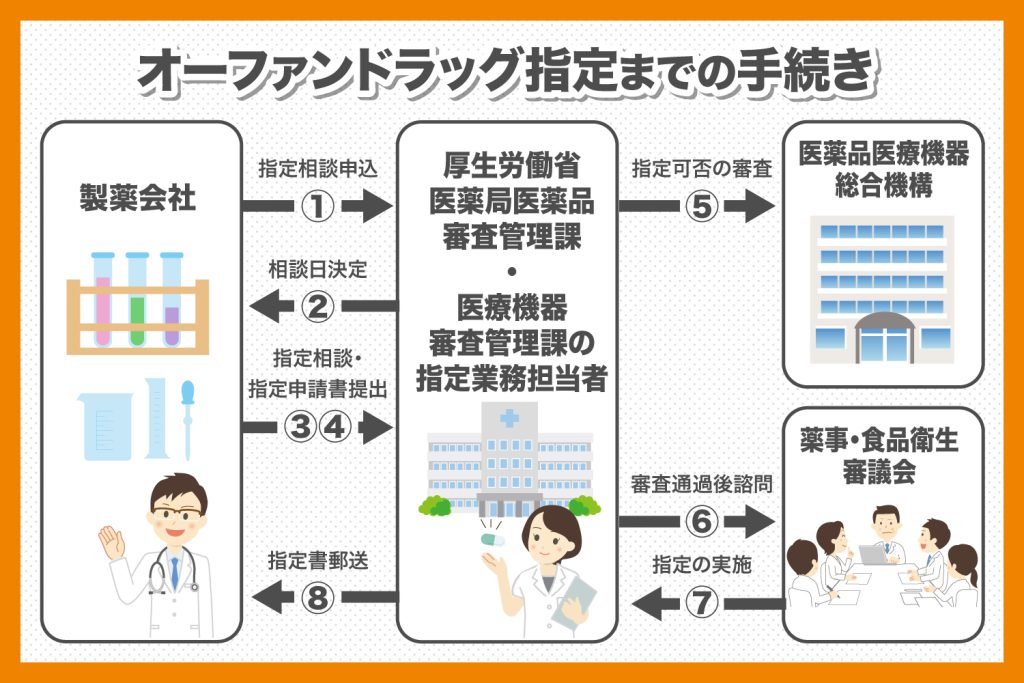
オーファンドラッグ指定を受けるには、所定の手続きがあります。 手続きの事前準備から申請までの流れをご紹介します。
- 厚生労働省医薬局医薬品審査管理課もしくは医療機器審査管理課の指定業務担当者にメール・郵送・FAXのいずれかで申し込み書類を提出し、指定相談の申し込みをする
- 指定業務担当者から相談日決定の通知を受ける
- 厚生労働省医薬局医薬品審査管理課もしくは医療機器審査管理課で、指定相談を行う
- 指定相談後、問題がなければ指定申請書を提出する
- 指定の可否についての審査が行われる
- 審査を通過した場合、薬事・食品衛生審議会で諮問が行われる
- 薬事・食品衛生審議会で行われる審議により、指定に問題がないと認められた場合、指定が実施される
- 各種手続きが終了したのち、申請者に指定書が郵送される
指定の手続きをする には、必ず指定相談をしなくては なりません。指定相談をする 際は、指定申請に必要な資料の案や、該当医薬品の説明が可能な資料などを用意する必要があります。
事前に資料を郵送するなどの対応をしなくてはならないケースもあるため、まずは厚生労働省医薬局医薬品審査管理課もしくは医療機器審査管理課の指定業務担当者に問い合わせ、不備がないように準備をしておきましょう。
近年承認されたオーファンドラッグの例
1993年に第1号となる「L-アルギニン及び塩酸Lアルギニンの混合物」が承認されて以来 、2024年3月21日時点で600品目がオーファンドラッグとして承認を受けています(※1)(※2)。近年指定を受けたオーファンドラッグの一例を見てみましょう。
| 指定日 | 医薬品の名称 | 効能もしくは効果 |
| 2023年12月22日 | アレクチニブ塩酸塩 | ALK 融合遺伝子陽性の非小細胞肺癌における術 後補助療法 |
| 2023年12月22日 | ボロファラン(10B) | 切除不能な皮膚血管肉腫 |
| 2023年12月22日 | イソトレチノイン | 神経芽腫 |
| 2023年12月22日 | ペムブロリズマブ(遺伝子組換え) | 高リスクの局所進行の子宮頸癌における同時化 学放射線療法 |
| 2023年12月22日 | テプロツムマブ(遺伝子組換え) | 甲状腺眼症 |
| 2024年2月9日 | Encaleret | 常染色体顕性(優性)低カルシウム血症 1型 |
| 2024年2月9日 | Tinlarebant | スタルガルト病 |
| 2024年2月9日 | ベルズチファン | フォン・ヒッペル・リンドウ(VHL)病関連の腫瘍性病変 |
| 2024年2月9日 | タルラタマブ(遺伝子組換え) | 小細胞肺癌 |
| 2023年3月21日 | Talquetamab | 多発性骨髄腫 |
| 2023年3月21日 | sotatercept | 肺動脈性肺高血圧症 |
| 2023年3月21日 | エフガルチギモド アルファ(遺伝子組換え) ボルヒアルロニダーゼ アルファ(遺伝子組換え) 配合注射剤 | 慢性炎症性脱髄性多発根神経炎 |
※1参考:厚生労働省.「希少疾病用医薬品指定品目一覧表(令和6年2月7日現在)」(2024-05-31).
※2参考:厚生労働省.「R2.9.1以降に希少疾病用医薬品に指定された品目一覧(令和6年3月21日時点)」(2024-05-31).
まとめ
オーファンドラッグ指定を受ければ、助成金や税制優遇措置が受けられる上、医薬品の承認審査が優先され、スムーズに医薬品の開発が進められるようになり、病気に苦しんでいる方の治療の選択肢が増えます。 該当する医薬品の開発を計画している場合は、少しでも必要な方に薬が届けられるように、オーファンドラッグ申請を検討してはいかがでしょうか。





